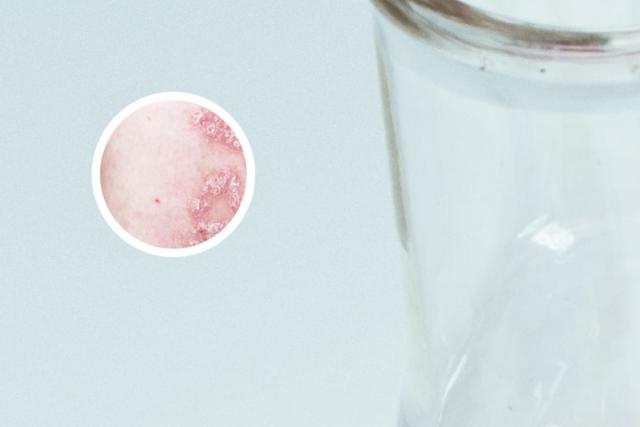
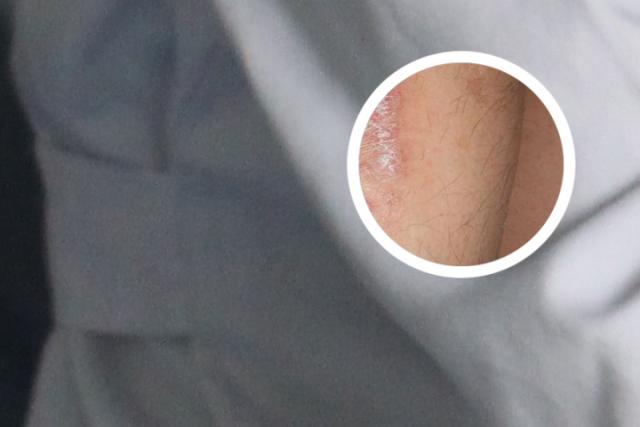
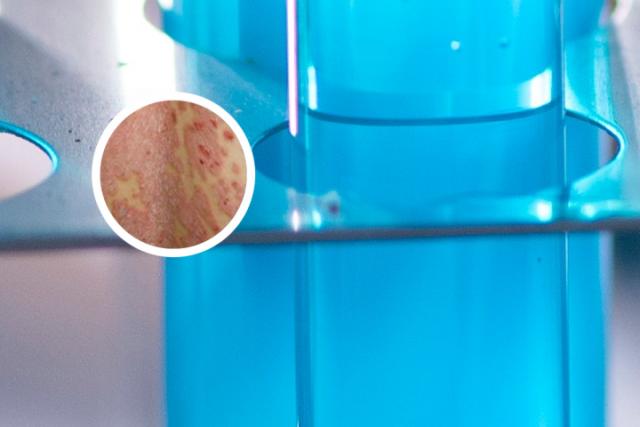
银屑病是一种自身免疫性疾病,常被认为是由遗传和环境等多因素共同作用而引起的。对于这种疾病,我们可以通过建立小鼠模型来深入研究。
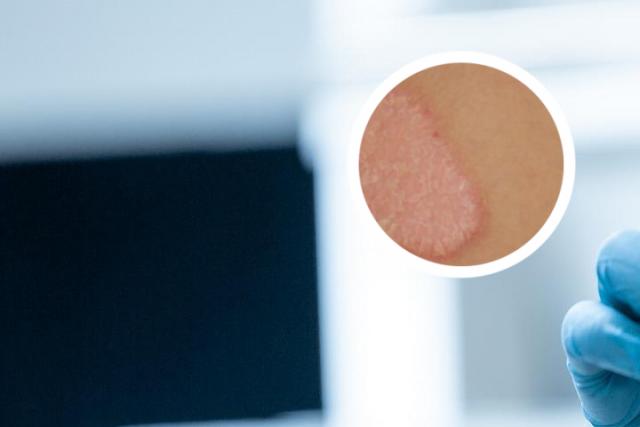
首先,我们需要确定适用于银屑病小鼠模型建立的小鼠品种。过去的研究表明,使用C57BL/6J小鼠品系建立的银屑病模型具有很高的可重复性和复杂性。此外,因为该品系小鼠在对抗自身免疫方面是较为薄弱的,所以使用该品系建立的银屑病模型可以更好地反映人类银屑病的病理特征。
接下来,我们需要考虑银屑病模型的诱导方式。简单的方法是采用化学或物理离子照射手段,这种方法能够生成较高质量的银屑病模型。同时,我们也可以考虑使用基因调控等技术来诱导银屑病模型。近年来,随着肠道菌群与银屑病之间的关联被越来越多的人所认知,通过调节肠道菌群来诱导银屑病小鼠模型的方法也备受关注。
在建立模型后,我们需要创造一个“银屑病环境”使得该疾病模型能够更好地得到复制。这通常可以通过完善银屑病标志物来达到。银屑病的标志物包括介素17、肿瘤坏死因子α、角质形成细胞及色素细胞表面标志等。
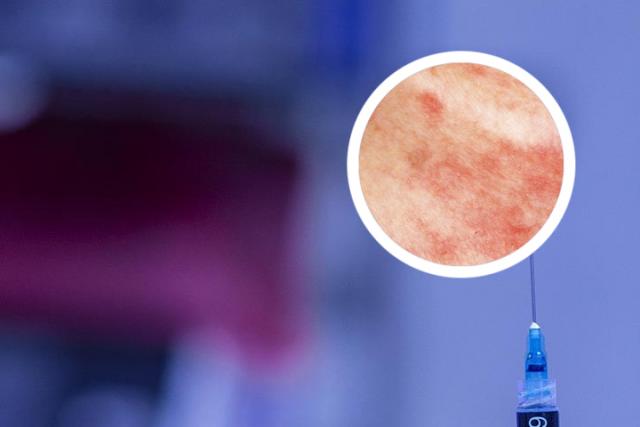
银屑病小鼠模型建立是一个复杂的过程,需要我们对小鼠品系、诱导方式以及模型环境等方面都进行充分考虑。只有找到最合适的方法,才能够更好地模拟真实的银屑病状态,为相关药物的研发提供必要的条件和指导。
小鼠银屑病耳朵模型
小鼠银屑病耳朵模型是一种常用的皮肤炎症模型,在皮肤病研究中有着广泛应用。该模型通过注射小鼠皮肤细胞中的杀伤细胞因子,以刺激皮肤细胞增殖和炎症反应,进而引起银屑病样皮损。
银屑病是一种常见的慢性自身免疫性疾病,其中患者体内的异常免疫反应引发手肘、膝盖、脊柱等部位出现皮肤损害。为了更好地了解银屑病表观遗传学的变化、不同基因的调节效应及其对疾病的影响,研究人员通常会选用小鼠银屑病耳朵模型进行实验。

小鼠银屑病耳朵模型的建立需要经过若干步骤。首先,采用吸嘴吸气法或其他途径麻醉小鼠,打开小鼠耳廓下方的机能敏感区,刮去表皮,并杀伤部分皮肤细胞。接着,向该区域注射诸如高浓度盐酸异丙肾上腺素、起炎药和多种至关重要的细胞因子,如经典cGAS / STING信号通路(cGAS:cGAMP合成酶;STING:刺激DNA的新型基因)可触发银屑病样反应。疾病模型随之出现,表现为具有银屑样斑块的角化不全和结构紊乱,同时伴有肉芽肿、淋巴细胞浸润等。
需要注意的是,小鼠银屑病耳朵模型还需考虑到诸多因素的干扰。例如,不同的小鼠品系、不同的年龄对模型的构建可能会产生影响。因此,在进行实验前应选择合适的动物品种和模型建立时间,以便取得更具说服力的实验结果。
小鼠银屑病耳朵模型准确、可靠地模拟了银屑病的病理过程,并已被广泛应用于皮肤炎症和自身免疫性疾病研究中。在实验前需要注意细节,以便获得准确的结果,有助于加深我们对这种皮肤病患者所面临的痛苦和疾病机制的认识。
银屑病小鼠模型
银屑病是一种常见的自身免疫性疾病,它通常表现为皮肤表面出现红斑、鳞屑和瘙痒等症状。目前,人们还不完全了解这种疾病的具体机制,因此需要进行更深入的研究和探索。为此,科学家们常常使用动物模型进行实验研究,其中银屑病小鼠模型就是其中之一。
首先,我们需要了解什么是动物模型。动物模型是指通过人工手段使实验动物病变,然后进行疾病研究的一种方法。因为这些实验动物的遗传背景、禽兽特征和生理功能等方面都与人类相似,所以可以在这些动物身上进行疾病发病机制的研究,来推断人类疾病的发病机理和治疗方法。
那么银屑病小鼠模型是如何建立的呢?目前,已有多种方法可以制造这种模型,其中最常用的是基因敲除和人类角质形成蛋白基因Tg。基因敲除技术是利用CRISPR/Cas9或其他方法,将小鼠中特定基因的DNA序列进行快速精准的编辑,达到敲除的目的,从而研究该基因与疾病的关系。而Tg则是指将人类角质形成蛋白基因导入到小鼠中,通过表达人类角质形成蛋白的方式来模拟银屑病的病变过程。
经过这些方法建立的银屑病小鼠模型,其病理学表现、分子机制、诊断方法、治疗效果等方面都与人类银屑病非常相似,对银屑病的研究具有重要的意义和价值。当前,许多科学家正致力于银屑病小鼠模型的深入研究,以期进一步了解这种疾病的发病机制和治疗方法,为银屑病的治疗带来新的突破和进展。